Отопление частного дома
Конвекторное отопление дома на сегодняшний день является наиболее оптимальным типом обогрева. Для того чтобы сделать обогрев частного дома максимально эффективным, необходимо правильно подобрать оборудование.
Лучше всего доверить подбор оборудования специалистам, но при желании это можно сделать и самостоятельно.
Действительно ли электроконвекторы для отопления частного дома являются выгодными, как правильно сделать все просчеты по подбору – расскажем ниже.
Выгода использования конвектора в частном домеЕсли рассматривать другие способы отопления дома, в котором не предполагается центрального отопления, то можно выделить несколько несомненных плюсов конвекторов:
- не нужно приобретать дорогие котлы, которые, к тому же, требуют больших вложений в монтаж оборудования;
- нет необходимости проводить тепловой контур из труб по всему периметру дома, что тоже значительно сократит издержки при расчете затрат на отопление;
- нет необходимости дополнительно приобретать датчики контроля температуры;
- не нужно заказывать дорогостоящие проекты по отоплению.

Таким образом, можно сделать вывод, что уже на первоначально этапе создания системы отопления в частном доме удастся значительно сократить издержки, за счет отсутствия необходимости покупать дорогостоящее оборудование и дополнительные материалы, оплачивать монтаж и т.д.
При расчете мощности электроконвекторов для частного дома предлагается руководствоваться стандартной формулой – 100 Вт на 1 м2. Но стоит отметить, что данная цифра достаточно условна, так как помимо метража помещения, на выбор мощности конвектора влияют и косвенные факторы, а именно – высота потолков, количество окон и их ориентация по сторонам света, качество теплоизоляции стен, возможность появления сквозняков, количество приборов, выделяющих тепло, количество людей, планирующих постоянно находиться в помещении и т.д. Все эти моменты важно предусмотреть заранее, для того чтобы в дальнейшем не оказалось, что приобретенное количество конвекторов не справляется с отоплением.
Помимо этого, электрические конвекторы для отопления дома позволяют экономить еще и за счет максимальной точности установки и поддержания температурного режима в помещении. В данном случае речь идет о современных конвекторах последнего поколения, которые способны поддерживать температуру с точностью до 0,4 С. Так, если в комнате требуется поддерживать температурный режим, например, в 22 С, то при нагревании конвектора до оптимальной температуры и при прогреве помещения до 22 С, конвектор отключится автоматически. Это значит, что он не будет работать впустую, расходуя электроэнергию. Как только температура начнет снова понижаться, конвектор продолжит нагревать помещение, не потеряв при этом ни одного Ватта энергии впустую.
В данном случае речь идет о современных конвекторах последнего поколения, которые способны поддерживать температуру с точностью до 0,4 С. Так, если в комнате требуется поддерживать температурный режим, например, в 22 С, то при нагревании конвектора до оптимальной температуры и при прогреве помещения до 22 С, конвектор отключится автоматически. Это значит, что он не будет работать впустую, расходуя электроэнергию. Как только температура начнет снова понижаться, конвектор продолжит нагревать помещение, не потеряв при этом ни одного Ватта энергии впустую.
Конвекторы, в зависимости от модели, могут иметь термостат, который поддерживает удаленное интеллектуальное управление. Приобретение таких конвекторов тоже позволит сэкономить при их эксплуатации. Рассмотрим, каким образом это делается.
При подключении конвектора к интеллектуальным системам управления пользователь получает возможность не только удаленно управлять конвектором, что само по себе очень удобно и функционально, но и задавать программы на один день, неделю или месяц.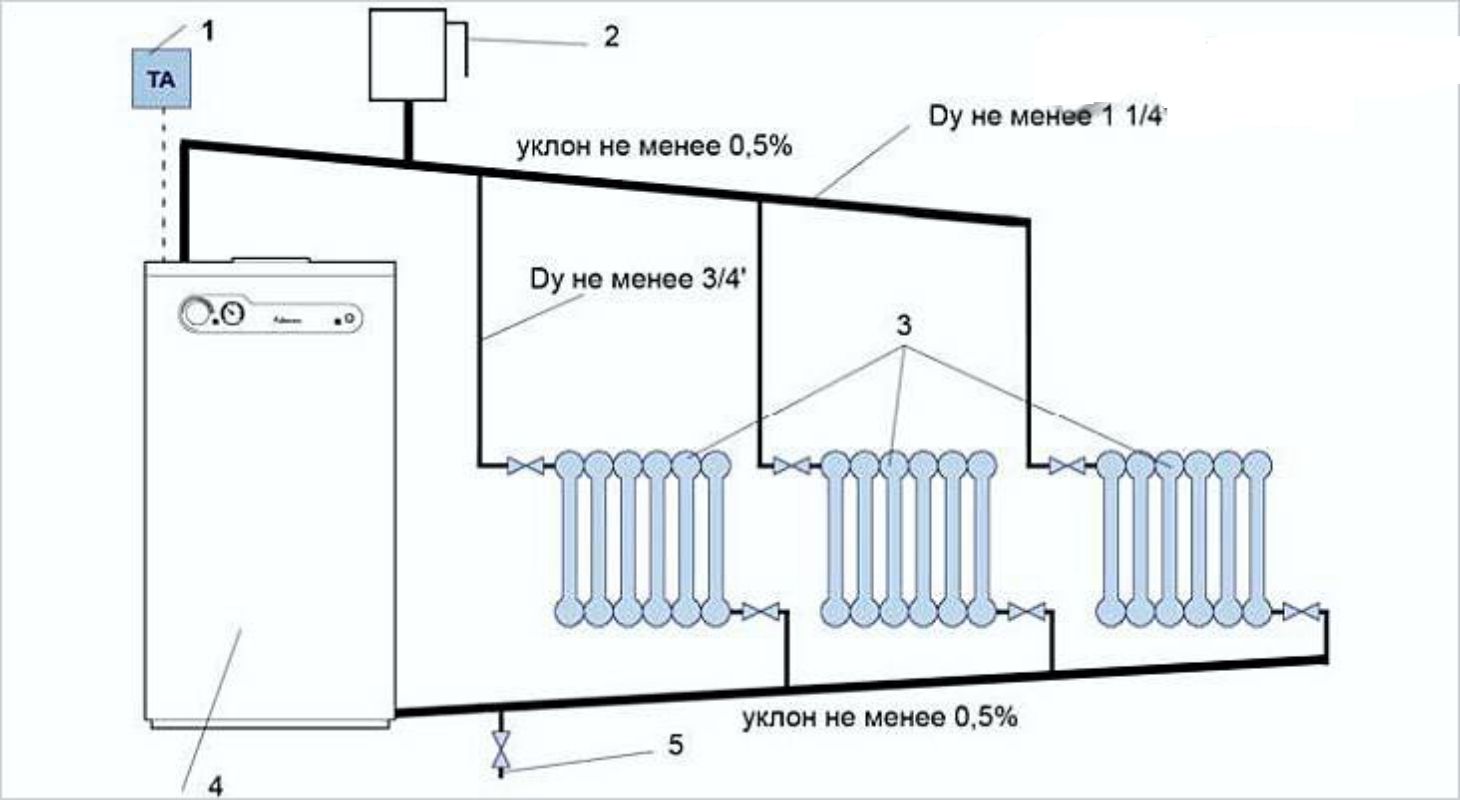
Также весьма удобна возможность задавать разные программы для разных зон в доме. Так для детской комнаты будут комфортны одни температурные показатели, а для зоны кухни – другие.
Помимо этого, дополнительной экономии будут способствовать минимальные затраты электроэнергии в режиме ожидания электроконвектора.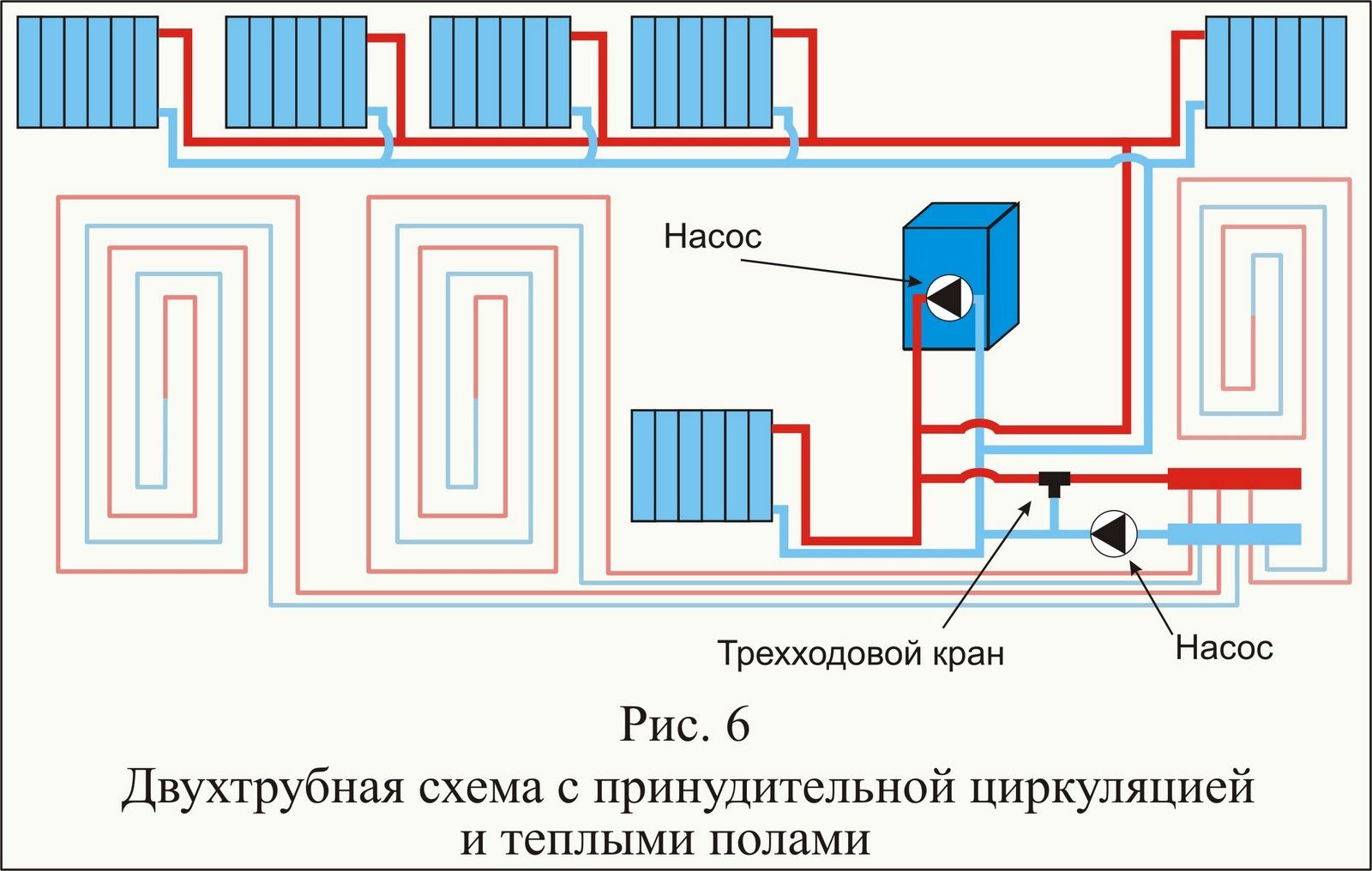
Точное количество конвекторов рассчитывается по формуле, написанной выше. Если помещение просторное, то потребуется больше конвекторов. Например, для комнаты в 20 м2 с хорошей теплоизоляцией, при обычной высоте потолков до 3 м можно обойтись даже 2 конвекторами по 500 Вт, но это условные цифры, так как в зависимости от прочих характеристик помещения может потребоваться либо больше конвекторов, либо сами конвекторы будут более мощными, например, по 1000 Вт. Для равномерного и быстрого распределения тепла конвекторы лучше располагать по всему периметру комнаты. Лучшим местом для установки конвекторов будет проем под окном, рядом со входом или рядом с местом отдыха. Не стоит устанавливать все приборы в одном углу комнаты, в этом случае воздух будет прогреваться неравномерно.
Конвекторы можно монтировать на стену при помощи креплений, которые продаются в комплекте, либо приобрести для них ножки и установить на полу. Плюс современных конвекторов в том, что они производятся в стильном лаконичном корпусе, и подойдут для помещения в любом дизайне. Благодаря их мобильности, конвекторы всего можно перенести в другое помещение без каких-либо проблем с демонтажем.
Расчет затрат на отоплениеДля того чтобы понимать затраты на электроэнергию, можно следовать следующим расчетам. На 1 м2 нужен конвектор 100 Вт. Из расчета всего количества конвекторов в доме нужно умножить их суммарное потребление электроэнергии на стоимость энергии в регионе (везде стоимость будет отличаться). Таким образом получится итоговая цифра, но она будет приблизительной, так как этот расчет предполагает круглосуточную работу конвектора на оптимальной мощности. С учетом же реального потребления сумма будет гораздо ниже, особенно, если установлен современный конвектор с возможностью программирования.
Как снизить затраты
Существует несколько способов снижения затрат при обогреве частного дома. Об этом лучше всего задуматься уже на этапе проектирования здания.
- Можно сделать дополнительную теплоизоляцию стен, это позволит дому меньше терять тепло.
- Стеклопакеты лучше всего ставить трех- или пятипрофильные, что позволит избежать теплопотери.
- Двери тоже влияют на теплопотери, для их минимизации лучше купить двери с теплоизолирующей прослойкой.
- Утепление подвала и чердака также позволит значительно сэкономить на обогреве.
Конвектор для отопления частного дома следует выбирать максимально тщательно – важно обратить внимание на следующие характеристики:
- мощность прибора;
- точность поддержания температуры;
- возможность программирования;
- безопасность – наличие автоотключения, защита от опрокидывания, минимальный нагрев корпуса и т.
 д.;
д.; - потребление энергии в спящем режиме;
- дизайн корпуса конвектора;
- гарантии производителя;
- ресурс работы.
При правильном выборе электроконвектора отопление в частном доме будет эффективным и бюджетным.
Вы знаете, что необходимо добавить тепло к веществу, чтобы увеличить его температуру, но вы можете не знать, что для изменения температуры определенного количества различных веществ на 1 градус Цельсия требуется разное количество тепловой энергии. Также требуется различное количество тепловой энергии для повышения температуры данного количества конкретного вещества в зависимости от того, является ли оно твердым, жидким или газообразным. Разным веществам также требуется разное количество тепловой энергии, чтобы превратить определенное их количество из твердого в жидкое или из жидкого в газообразное. Показ того, как мы описываем эти вещи количественно, поможет прояснить это. Теплоемкость — это количество тепла, которое увеличивает температуру данного объекта на один градус Цельсия или один кельвин. (Помните, что величина градуса Цельсия такая же, как и одного кельвина). Объект может быть чистым соединением или элементом, или это может быть смесь веществ. Наиболее распространенной переменной теплоемкости является заглавная буква C , а наиболее распространенными единицами измерения являются Дж/°C, Дж/К, кДж/°C или кДж/К. Следующая формула показывает, как рассчитать количество тепла, необходимое для повышения температуры объекта на определенное изменение температуры ( ΔT ). Мы используем строчные буквы q для обозначения тепловой энергии. q = С ⋅ ΔT ΔT = T 2 – T 1 Для чистых элементов и соединений более полезна удельная теплоемкость. Удельная теплоемкость (часто называемая просто удельной теплоемкостью ) — это количество тепловой энергии (обычно в джоулях), необходимое для повышения температуры одного грамма вещества на один градус Цельсия или один кельвин. q = м ⋅ c ⋅ ΔT Ниже приведена таблица некоторых общих удельных теплоемкостей при постоянном давлении и 25 °C, если не указано иное.
Обратите внимание, что существуют значительные различия в удельной теплоемкости, и обратите внимание, что одно и то же вещество (в данном случае вода) имеет разную удельную теплоемкость в зависимости от того, является ли оно твердым, жидким или газообразным. Также обратите внимание, что жидкая вода имеет особенно высокую удельную теплоемкость. | Теперь рассмотрим энергию, связанную с фазовым переходом твердого тела в жидкое (плавление). Теплота плавления , ΔH fus , это тепловая энергия, необходимая для преобразования данного количества твердого вещества в жидкость при постоянном давлении. q = м ⋅ ΔH фуз Превращение жидкости в твердое (затвердевание) прямо противоположно превращению твердого тела в жидкость (плавление), поэтому теплота затвердевания ΔH затвердевание , прямо противоположно теплу синтеза. Например, теплота затвердевания воды составляет -333,55 Дж/г. ( ΔH для поглощенной энергии, например, для процесса плавления, описывается как положительное значение, а ΔH для высвобождаемой энергии, например, для процесса затвердевания, описывается как отрицательное. Далее рассмотрим энергию, связанную с фазовым переходом жидкости в газ (кипение или испарение). Теплота парообразования , ΔH vap , тепловая энергия, необходимая для преобразования данного количества жидкости в газ при постоянном давлении. Как и для ΔH fus , ΔHvap обычно описывается в Дж/г. Как и в случае с теплотами плавления, теплоты парообразования варьируются от одного вещества к другому. Например, для воды она составляет 2257 Дж/г, для ацетона — 538,9 Дж/г, для метана — 480,6 Дж/г. Обратите внимание, что вода имеет относительно высокую теплоту парообразования по сравнению с другими и что теплота парообразования значительно выше, чем теплота плавления для каждого вещества. Следующее уравнение можно использовать для расчета тепловой энергии, связанной с процессом парообразования. q = м ⋅ ΔH пар Превращение газа в жидкость (конденсация) прямо противоположно превращению жидкости в газ (испарение), поэтому теплота конденсации, ΔH конденсация , прямо противоположна теплоте парообразования. Теперь давайте рассмотрим изменения, которые претерпевает вещество, такое как вода, по мере того, как тепло постоянно добавляется к твердой форме вещества. См. изображение ниже. Сначала добавление тепла увеличивает температуру твердого тела. Мы могли бы провести расчеты для этой стадии, используя уравнение удельной теплоемкости, включающее удельную теплоемкость твердого тела ( с с ). q = м ⋅ c с ⋅ ΔT Когда температура достигает точки плавления вещества (0 °C для воды), вещество начинает плавиться. В то время как твердое тело все еще превращается в жидкость, температура остается постоянной, потому что добавленная энергия преобразуется в потенциальную энергию, а не в кинетическую энергию. Процесс плавления нарушает некоторые притяжения между частицами, а более слабое притяжение между частицами в жидкости делает жидкость менее стабильной и имеет более высокую потенциальную энергию, чем твердое тело. q = м ⋅ ΔH фуз Когда все твердое тело превращается в жидкость, добавленная энергия идет на увеличение кинетической энергии и, следовательно, температуры вещества. Мы могли бы провести расчеты для этой стадии, используя уравнение удельной теплоемкости, включающее удельную теплоемкость жидкости ( c l ). q = м ⋅ с л ⋅ ΔT Когда температура достигает точки кипения вещества (100 °C для воды), вещество начинает кипеть и жидкость превращается в газ. В то время как жидкость все еще превращается в газ, температура остается постоянной, потому что, опять же, добавленная энергия преобразуется в потенциальную энергию, а не в кинетическую энергию. q = м ⋅ ΔH пар Когда вся жидкость превращается в газ, добавленная энергия идет на увеличение кинетической энергии и, следовательно, температуры вещества. Мы могли бы провести расчеты для этой стадии, используя уравнение удельной теплоемкости, которое включает удельную теплоемкость газа ( c г ). q = м ⋅ с г ⋅ ΔT На изображении ниже показаны переходы от твердого к жидкому и к газообразному, от газа к жидкому и к твердому. |
11.3 Фазовый переход и скрытая теплота — физика
Раздел Цели обучения
К концу этого раздела вы сможете делать следующее:
- Объяснять изменения теплоты при изменении состояния и описывать скрытые теплоты плавления и парообразования
- Решение задач, связанных с изменением тепловой энергии при нагревании и охлаждении веществ с фазовыми переходами
Поддержка учителей
Поддержка учителей
Цели обучения в этом разделе помогут вашим учащимся освоить следующие стандарты:
- (6) Научные концепции.
 Учащийся знает, что изменения происходят в физической системе, и применяет законы сохранения энергии и импульса. Ожидается, что студент:
Учащийся знает, что изменения происходят в физической системе, и применяет законы сохранения энергии и импульса. Ожидается, что студент:- (Э) описать, как макроскопические свойства термодинамической системы, такие как температура, удельная теплоемкость и давление, связаны с молекулярным уровнем материи, включая кинетическую или потенциальную энергию атомов;
- (Ф) противопоставить и привести примеры различных процессов переноса тепловой энергии, включая теплопроводность, конвекцию и излучение.
Основные термины раздела
| конденсат | замораживание | скрытая теплота | сублимация |
| скрытая теплота плавления | скрытая теплота парообразования | плавка | испарение |
| изменение фазы | фазовая диаграмма | плазма |
Поддержка учителей
Поддержка учителей
В начале этого раздела попросите учащихся привести примеры твердых тел, жидкостей и газов.
Фазовые изменения
До сих пор мы узнали, что добавление тепловой энергии за счет тепла увеличивает температуру вещества. Но как ни удивительно, бывают ситуации, когда добавление энергии вообще не меняет температуру вещества! Вместо этого дополнительная тепловая энергия ослабляет связи между молекулами или атомами и вызывает фазовый переход. Поскольку эта энергия входит или выходит из системы во время фазового перехода, не вызывая изменения температуры в системе, она известна как скрытая теплота (скрытая означает скрытый ).
Вы часто сталкиваетесь с тремя фазами материи: твердой, жидкой и газообразной (см. рис. 11.8). Твердое тело имеет наименее энергетическое состояние; атомы в твердых телах находятся в тесном контакте, между ними действуют силы, которые позволяют частицам вибрировать, но не менять положение с соседними частицами. (Эти силы можно представить себе как пружины, которые можно растянуть или сжать, но их нелегко сломать. )
)
Жидкость имеет более энергетическое состояние, в котором частицы могут плавно скользить друг мимо друга и менять соседей, хотя они все еще удерживаются вместе за счет взаимного притяжения.
Газ имеет более энергетическое состояние, чем жидкость, в котором частицы разрываются от своих связей. Частицы в газах разделены расстояниями, большими по сравнению с размером частиц.
Наиболее энергичным состоянием является плазма. Хотя вы, возможно, мало что слышали о плазме, на самом деле это наиболее распространенное состояние материи во Вселенной — звезды состоят из плазмы, как и молнии. Состояние плазмы достигается путем нагревания газа до точки, в которой частицы разрываются, отделяя электроны от остальной части частицы. При этом образуется ионизированный газ, представляющий собой комбинацию отрицательно заряженных свободных электронов и положительно заряженных ионов, известный как плазма.
Рисунок
11,8
(а) Частицы в твердом теле всегда имеют одних и тех же соседей, удерживаемых рядом силами, представленными здесь пружинами.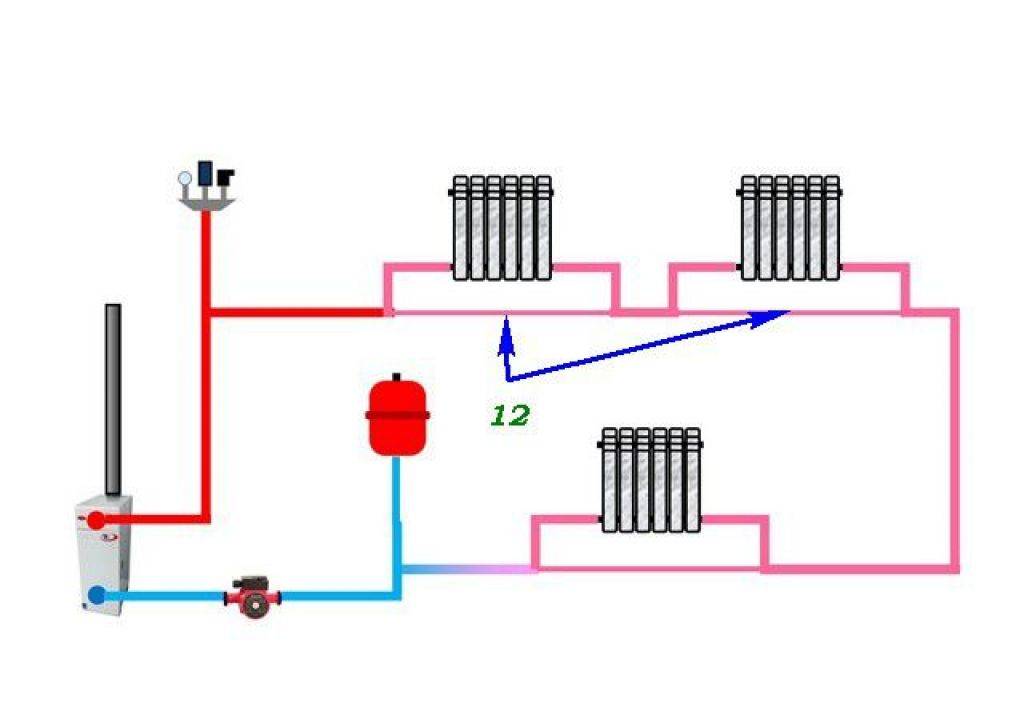 Эти частицы по существу находятся в контакте друг с другом. Камень является примером твердого тела. Эта порода сохраняет свою форму из-за сил, удерживающих ее атомы или молекулы вместе. б) Частицы в жидкости также находятся в тесном контакте, но могут скользить друг по другу. Силы между ними сильно сопротивляются попыткам сблизить их, а также удержать в тесном контакте. Вода является примером жидкости. Вода может течь, но она также остается в открытом сосуде из-за сил между ее молекулами. в) Частицы в газе разделены расстояниями, значительно превышающими размеры самих частиц, и они свободно перемещаются. Газ должен находиться в закрытом контейнере, чтобы предотвратить его выход в окружающую среду. (d) Атмосфера ионизируется при сильном нагреве удара молнии.
Эти частицы по существу находятся в контакте друг с другом. Камень является примером твердого тела. Эта порода сохраняет свою форму из-за сил, удерживающих ее атомы или молекулы вместе. б) Частицы в жидкости также находятся в тесном контакте, но могут скользить друг по другу. Силы между ними сильно сопротивляются попыткам сблизить их, а также удержать в тесном контакте. Вода является примером жидкости. Вода может течь, но она также остается в открытом сосуде из-за сил между ее молекулами. в) Частицы в газе разделены расстояниями, значительно превышающими размеры самих частиц, и они свободно перемещаются. Газ должен находиться в закрытом контейнере, чтобы предотвратить его выход в окружающую среду. (d) Атмосфера ионизируется при сильном нагреве удара молнии.
При фазовом переходе материя переходит из одной фазы в другую либо за счет добавления энергии за счет тепла и перехода в более энергетическое состояние, либо за счет удаления энергии за счет тепла и перехода в менее энергетическое состояние.
Фазовые переходы в более энергичное состояние включают следующее:
- Плавление — из твердого состояния в жидкое
- Испарение — превращение жидкости в газ (включая кипение и испарение)
- Сублимация — превращение твердого вещества в газ
- ИонизацияГаз в плазму
Фазовые переходы в менее энергетическое состояние следующие:
- Конденсация — газ в жидкость
- Замораживание — переход из жидкого состояния в твердое
- Рекомбинация — превращение плазмы в газ
- Осаждение из газа в твердое вещество
Для плавления твердого тела требуется энергия, потому что связи между частицами в твердом теле должны быть разрушены. Поскольку энергия, связанная с фазовыми переходами, используется для разрыва связей, кинетическая энергия частиц не увеличивается и, следовательно, не повышается температура. Точно так же энергия необходима для испарения жидкости, чтобы преодолеть силы притяжения между частицами в жидкости. Изменение температуры не происходит до тех пор, пока не завершится фазовый переход. Температура чашки газировки и льда, которая изначально была равна 0°C°C, остается на уровне 0°C°C до тех пор, пока весь лед не растает. В противоположность этим процессам — замерзанию и конденсации — из скрытой теплоты высвобождается энергия (см. рис. 11.9).).
Изменение температуры не происходит до тех пор, пока не завершится фазовый переход. Температура чашки газировки и льда, которая изначально была равна 0°C°C, остается на уровне 0°C°C до тех пор, пока весь лед не растает. В противоположность этим процессам — замерзанию и конденсации — из скрытой теплоты высвобождается энергия (см. рис. 11.9).).
Поддержка учителей
Поддержка учителей
[BL][OL] Спросите учащихся, одинаковое ли количество энергии поглощается или выделяется при плавлении или замерзании определенного количества вещества.
[AL] Спросите учащихся, как вода может испаряться, даже если она имеет комнатную температуру, а не 100 °C°C.
Рисунок
11,9
(а) Энергия требуется для частичного преодоления сил притяжения между частицами в твердом теле с образованием жидкости. Та же самая энергия должна быть удалена, чтобы произошло замораживание. (б) Частицы разделены большими расстояниями при переходе из жидкости в пар, что требует значительной энергии для преодоления молекулярного притяжения.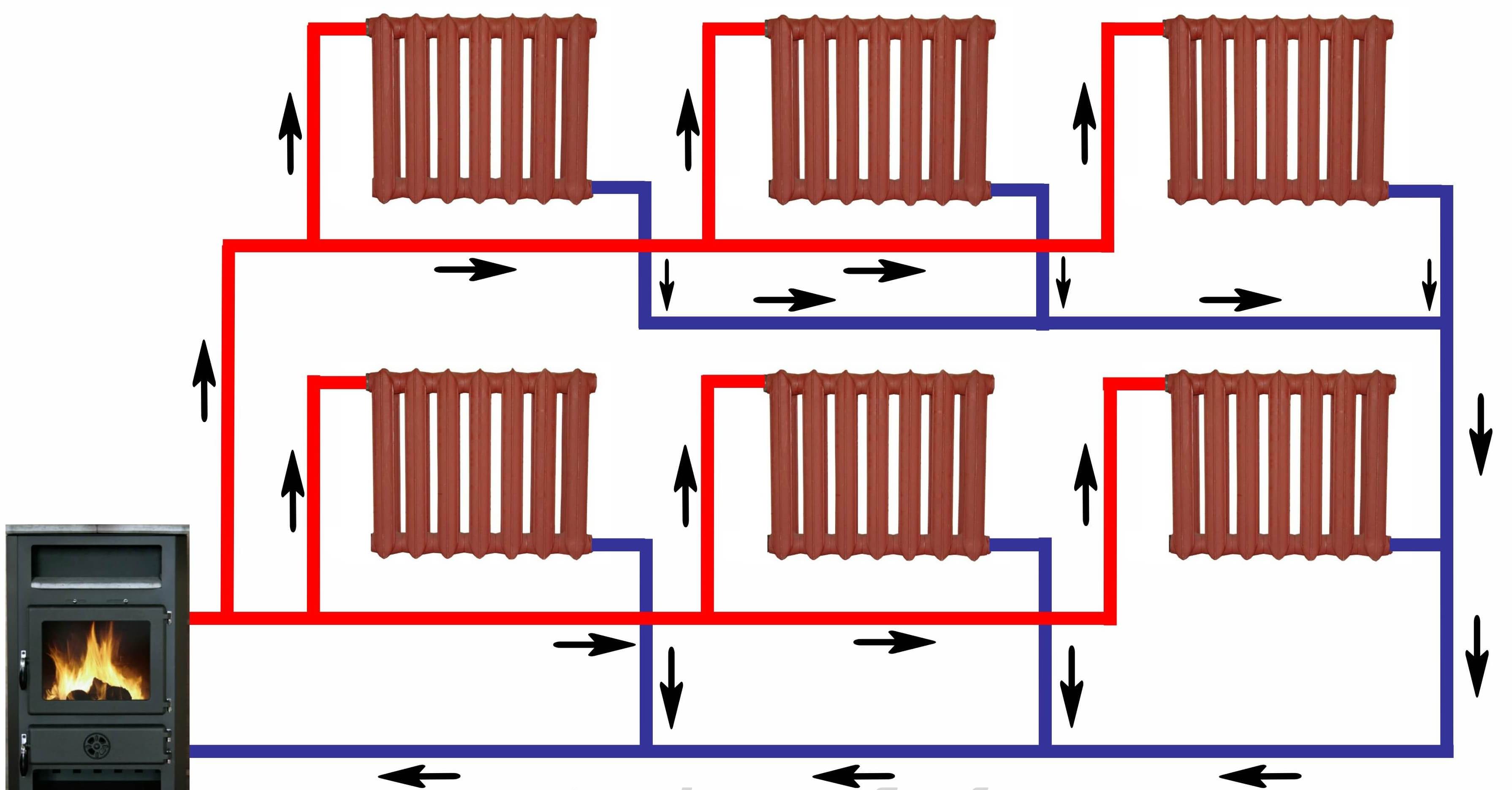 Такая же энергия должна быть удалена, чтобы произошла конденсация. Изменение температуры не происходит до тех пор, пока не завершится фазовый переход. (c) Энергии добавляется достаточно, чтобы полностью пропустить жидкое состояние, когда вещество подвергается сублимации.
Такая же энергия должна быть удалена, чтобы произошла конденсация. Изменение температуры не происходит до тех пор, пока не завершится фазовый переход. (c) Энергии добавляется достаточно, чтобы полностью пропустить жидкое состояние, когда вещество подвергается сублимации.
Теплота, Q , необходимая для изменения фазы образца массой м равна
Q=mLfQ=mLf (для плавления/замерзания),
Q=mLvQ=mLv (для парообразования/конденсации),
, где LfLf — скрытая теплота плавления, а LvLv — скрытая теплота парообразования. Скрытая теплота плавления – это количество тепла, необходимое для того, чтобы вызвать фазовый переход между твердым телом и жидкостью. Скрытая теплота парообразования – это количество тепла, необходимое для фазового перехода между жидкостью и газом. LfLf и LvLv — это коэффициенты, которые варьируются от вещества к веществу в зависимости от силы межмолекулярных сил, и оба имеют стандартные единицы Дж/кг. См. Таблицу 11.3 для значений LfLf и LvLv различных веществ.
См. Таблицу 11.3 для значений LfLf и LvLv различных веществ.
| Вещество | Точка плавления ( °C°C ) | Lf (кДж/кг) | Точка кипения ( °C°C ) | Lv (кДж/кг) |
|---|---|---|---|---|
| Гелий | ‒269,7 | 5,23 | ‒268,9 | 20,9 |
| Водород | ‒259,3 | 58,6 | ‒252,9 | 452 |
| Азот | ‒210,0 | 25,5 | ‒195,8 | 201 |
| Кислород | ‒218,8 | 13,8 | ‒183,0 | 213 |
| Этанол | ‒114 | 104 | 78,3 | 854 |
| Аммиак | ‒78 | 332 | ‒33,4 | 1370 |
| Меркурий | ‒38,9 | 11,8 | 357 | 272 |
| Вода | 0,00 | 334 | 100,0 | 2256 |
| Сера | 119 | 38,1 | 444,6 | 326 |
| Свинец | 327 | 24,5 | 1750 | 871 |
| Сурьма | 631 | 165 | 1440 | 561 |
| Алюминий | 660 | 380 | 2520 | 11400 |
| Серебро | 961 | 88,3 | 2193 | 2336 |
| Золото | 1063 | 64,5 | 2660 | 1578 |
| Медь | 1083 | 134 | 2595 | 5069 |
| Уран | 1133 | 84 | 3900 | 1900 |
| Вольфрам | 3410 | 184 | 5900 | 4810 |
Стол
11. 3
Скрытые теплоты плавления и испарения, а также температуры плавления и кипения
3
Скрытые теплоты плавления и испарения, а также температуры плавления и кипения
Давайте рассмотрим пример добавления тепла ко льду, чтобы изучить его переходы через все три фазы — из твердого состояния в жидкое и в газообразное. Фазовая диаграмма, показывающая изменения температуры воды при добавлении энергии, показана на рис. 11.10. Лед зарождается при температуре -20°C°C, и его температура линейно растет, поглощая тепло с постоянной скоростью, пока не достигнет 0°.°. При такой температуре лед постепенно тает, поглощая 334 кДж/кг. Температура остается постоянной на уровне 0°C°C во время этого фазового перехода. Как только весь лед растаял, температура жидкой воды повышается, поглощая тепло с новой постоянной скоростью. При 100°C°C вода начинает кипеть, и температура снова остается постоянной, а вода поглощает 2256 кДж/кг во время этого фазового перехода. Когда вся жидкость превратилась в пар, температура снова повышается с постоянной скоростью.
Рисунок
11.10
График зависимости температуры от добавленной энергии.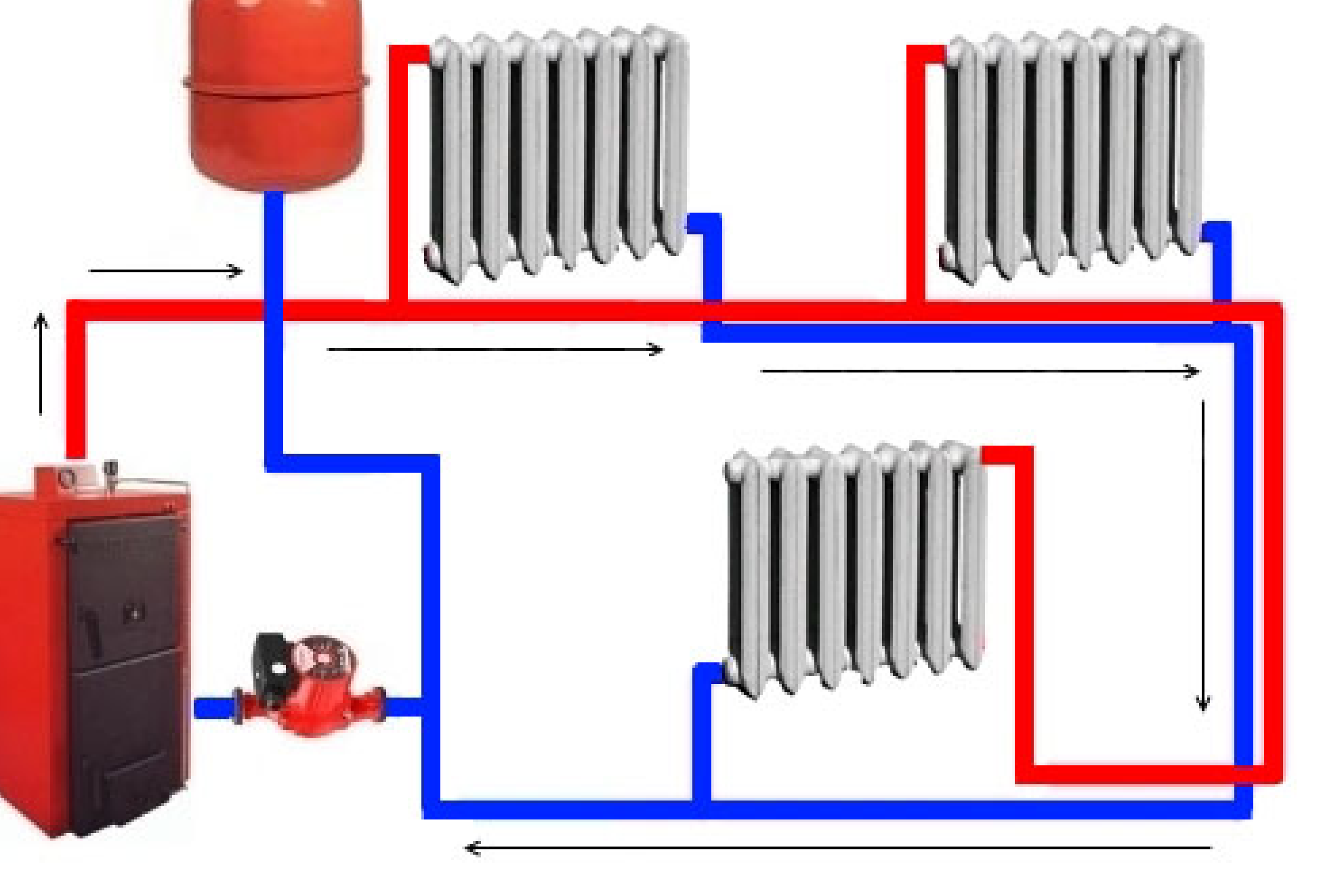 Система сконструирована таким образом, что при нагревании льда и превращении его в жидкую воду пар не образуется, поэтому при испарении пар остается в системе. Длинные участки постоянных значений температуры при 0°C°C и 100°C°C отражают большие скрытые теплоты плавления и испарения соответственно.
Система сконструирована таким образом, что при нагревании льда и превращении его в жидкую воду пар не образуется, поэтому при испарении пар остается в системе. Длинные участки постоянных значений температуры при 0°C°C и 100°C°C отражают большие скрытые теплоты плавления и испарения соответственно.
Мы видели, что испарение требует передачи тепла веществу из окружающей среды. Конденсация – это обратный процесс, при котором тепло передается от вещества до его окружения. Это выделение скрытой теплоты увеличивает температуру окружающей среды. Энергия должна быть удалена от конденсирующихся частиц, чтобы пар конденсировался. Вот почему на холодных поверхностях происходит конденсация: тепло передает энергию от теплого пара к холодной поверхности. Энергия точно такая же, как требуется для фазового перехода в другом направлении, от жидкости к пару, поэтому ее можно рассчитать по формуле Q=mLvQ=mLv. Скрытое тепло также выделяется в окружающую среду при замерзании жидкости и может быть рассчитано по формуле Q=mLfQ=mLf .
Веселье в физике
Приготовление мороженого
Рисунок 11.11 С подходящими ингредиентами, льдом и парой пластиковых пакетов вы могли бы сделать собственное мороженое за пять минут. (ElinorD, Wikimedia Commons)
Мороженое, конечно, достаточно легко купить в супермаркете, но для закоренелых энтузиастов мороженого это может быть недостаточно. Процесс изготовления собственного мороженого позволит вам изобретать собственные вкусы и воочию восхищаться физикой (рис. 11.11).
Первый шаг к приготовлению домашнего мороженого — это смешать жирные сливки, цельное молоко, сахар и вкус по вашему выбору; это может быть как просто какао-порошок или экстракт ванили, так и изысканно, как гранаты или фисташки.
Следующий шаг — перелить смесь в емкость, достаточно глубокую, чтобы вы могли взбивать смесь, не расплескивая ее, а также ее можно хранить в морозильной камере. После помещения в морозильную камеру мороженое необходимо энергично перемешивать каждые 45 минут в течение четырех-пяти часов. Это замедляет процесс замораживания и предотвращает превращение мороженого в сплошную глыбу льда. Большинство людей предпочитают мягкую кремовую текстуру вместо одного гигантского эскимо.
Это замедляет процесс замораживания и предотвращает превращение мороженого в сплошную глыбу льда. Большинство людей предпочитают мягкую кремовую текстуру вместо одного гигантского эскимо.
По мере замерзания сливки претерпевают фазовый переход от жидкого к твердому. К настоящему времени мы достаточно опытны, чтобы понять, что это означает, что сливки должны испытывать потерю тепла. Куда уходит это тепло? Из-за разницы температур между морозильной камерой и смесью для мороженого происходит передача тепловой энергии от мороженого воздуху в морозильной камере. Как только температура в морозильной камере достаточно повышается, морозильная камера охлаждается за счет откачки избыточного тепла наружу на кухню.
Более быстрый способ сделать мороженое — охладить его, поместив смесь в пластиковый пакет, окруженный другим пластиковым пакетом, наполовину заполненным льдом. (Вы также можете добавить чайную ложку соли во внешний пакет, чтобы понизить температуру смеси льда и соли.) Если встряхнуть пакет в течение пяти минут, мороженое взбивается и охлаждается равномерно. В этом случае тепло передает энергию от смеси мороженого льду во время фазового перехода.
В этом случае тепло передает энергию от смеси мороженого льду во время фазового перехода.
В этом видеоролике показано, как приготовить домашнее мороженое из льда и пластиковых пакетов.
Почему метод приготовления мороженого в пакетах со льдом работает намного быстрее, чем метод замораживания?
Лед имеет меньшую удельную теплоемкость, чем окружающий воздух в морозильной камере. Следовательно, он поглощает больше энергии из смеси мороженого.
Лед имеет меньшую удельную теплоемкость, чем окружающий воздух в морозильной камере. Следовательно, он поглощает меньше энергии из смеси мороженого.
Лед имеет более высокую удельную теплоемкость, чем окружающий воздух в морозильной камере.
 Следовательно, он поглощает больше энергии из смеси мороженого.
Следовательно, он поглощает больше энергии из смеси мороженого.Лед имеет более высокую удельную теплоемкость, чем окружающий воздух в морозильной камере. Следовательно, он поглощает меньше энергии из смеси мороженого.
Решение задач тепловой энергии с фазовыми переходами
Рабочий пример
Расчет тепла, необходимого для фазового перехода
Рассчитайте а) сколько энергии необходимо для растапливания 1000 кг льда при 0 °С°С (точка замерзания) и б) сколько энергии требуется для испарения 1000 кг воды при 100 °С°С (точка кипения ).
Стратегия ЗА (А)
Используя уравнение для теплоты, необходимой для плавления, и значение скрытой теплоты плавления воды из предыдущей таблицы, мы можем решить для части (а).
Раствор (a)
Энергия для таяния 1000 кг льда равна
Q=mLf=(1000 кг)(334 кДж/кг)=334 кДж. Q=mLf=(1000 кг)(334 кДж/кг )=334 кДж.
11.18
Стратегия ЗА (Б)
Чтобы решить часть (b), мы используем уравнение для теплоты, необходимой для парообразования, вместе со скрытой теплотой парообразования воды из предыдущей таблицы.
Решение (b)
Энергия испарения 1000 кг жидкой воды составляет
Q=mLv=(1000 кг)(2256 кДж/кг)=2256 кДж. Q=mLv=(1 000 кг)(2256 кДж/ кг)=2256 кДж.
11.19
Обсуждение
Количество энергии, необходимое для плавления килограмма льда (334 кДж), равно количеству энергии, необходимому для повышения температуры 1000 кг жидкой воды с 0 °C°C до 79,8 °C. °С. Этот пример показывает, что энергия фазового перехода огромна по сравнению с энергией, связанной с изменением температуры. Это также демонстрирует, что количество энергии, необходимое для испарения, еще больше.
Рабочий пример
Расчет конечной температуры по фазовому переходу: охлаждение газировки кубиками льда
Кубики льда используются для охлаждения газированных напитков при температуре 20 °C°C и массе msoda=0,25 кгmsoda=0,25 кг. Лед имеет температуру 0 °C°C, а общая масса кубиков льда составляет 0,018 кг. Предположим, что газировка хранится в контейнере из пеноматериала, так что потерями тепла можно пренебречь, и что газировка имеет ту же удельную теплоемкость, что и вода. Найдите конечную температуру, когда весь лед растает.
Стратегия
Кубики льда имеют температуру плавления 0 °C°C. Тепло передается от газировки льду для плавления. Плавление льда происходит в два этапа: сначала происходит фазовый переход и твердое тело (лед) превращается в жидкую воду при температуре плавления; затем температура этой воды повышается. При плавлении получается вода с температурой 0°C°C, поэтому от соды к этой воде передается больше тепла, пока они не станут одинаковой температуры. Так как количество тепла, отдаваемое газировке, равно количеству тепла, переданному льду.
Так как количество тепла, отдаваемое газировке, равно количеству тепла, переданному льду.
Qice=-QsodaQice=-Qsoda
11.20
Тепло, переданное льду, идет частично на фазовый переход (плавление), а частично на повышение температуры после таяния. Вспомним из предыдущего раздела, что отношение между теплотой и изменением температуры Q=mcΔTQ=mcΔT. Для льда изменение температуры равно Tf−0°CTf−0°C. Таким образом, общее тепло, переданное льду, равно
Qice=мышиLf+мышиw(Tf-0°C).Qice=мышиLf+мышиw(Tf-0°C).
11.21
Поскольку сода не меняет фазы, а только температуру, теплота, выделяемая содой, равна
Qsoda=msodacw(Tf−20°C).Qsoda=msodacw(Tf−20°C).
11.22
Так как Qice=-QsodaQice=-Qsoda,
мышейLf+мышиcw(Tf-0°C)=-msodacw(Tf-20°C).мышиLf+мышиcw(Tf-0°C)=-msodacw (Тф-20°С).
11,23
Перенося все члены, включающие TfTf, в левую часть уравнения, а все остальные члены в правую часть, мы можем найти TfTf .
Tf=msodacw(20°C)-мышиLf(msoda+мыши)cwTf=msodacw(20°C)-мышиLf(msoda+мыши)cw
11,24
Замена известных количеств
Tf=(0,25 кг)( 4186 Дж/кг⋅°C)(20°C)−(0,018 кг)(334 000 Дж/кг)(0,25 кг+0,018 кг)(4186 K/кг⋅°C)=13°CTf=(0,25 кг)( 4186 Дж/кг⋅°C)(20°C)−(0,018 кг)(334 000 Дж/кг)(0,25 кг + 0,018 кг)(4186 K/кг⋅°C)=13°C
11,25
Обсуждение
Этот пример показывает огромные энергии, связанные с изменением фазы. Масса льда составляет около 7 процентов от массы содовой, но это вызывает заметное изменение температуры содовой.
Советы для успеха
Если бы лед еще не достиг точки замерзания, нам также пришлось бы учитывать, сколько энергии потребуется для повышения его температуры до 0 °C°C до того, как произойдет фазовый переход. Это был бы реалистичный сценарий, потому что температура льда часто бывает ниже 0 °C°C.
Практические задачи
11.
Сколько энергии необходимо, чтобы растопить 2,00 кг льда при 0 °C?
- 334 кДж
- 336 кДж
- 167 кДж
- 668 кДж
12.
Если 2500\,\text{кДж} энергии достаточно, чтобы расплавить 3,0\,\text{кг} вещества, какова скрытая теплота плавления этого вещества?
7500\,\text{кДж} \cdot \text{кг}
7500\,\text{кДж/кг}
830\,\text{кДж} \cdot \text{кг}
830\,\text{кДж/кг}
Проверьте свое понимание
Поддержка учителей
Поддержка учителей
Используйте эти вопросы, чтобы оценить достижение учащимися учебных целей раздела. Если учащиеся борются с определенной целью, эти вопросы помогут определить, какая именно, и направить учащихся к соответствующему содержанию.
Если учащиеся борются с определенной целью, эти вопросы помогут определить, какая именно, и направить учащихся к соответствующему содержанию.
13.
Что такое скрытая теплота?
Это тепло, которое должно передавать энергию в систему или из системы, чтобы вызвать изменение массы при небольшом изменении температуры системы.
Это тепло, которое должно передавать энергию в систему или из системы, чтобы вызвать изменение массы без изменения температуры в системе.
Это тепло, которое должно передавать энергию в систему или из системы, чтобы вызвать фазовый переход при небольшом изменении температуры системы.



 д.;
д.;
 Наиболее распространенная переменная для удельной теплоемкости – строчная буква 9.0010 c
Наиболее распространенная переменная для удельной теплоемкости – строчная буква 9.0010 c  1813
1813 (В этом контексте плавление – это другое слово для плавления.) Единицы для ΔH fus различаются, но обычно они описываются в Дж / г. Как и удельные теплоемкости, теплоты плавления варьируются от одного вещества к другому. Например, для воды она составляет 333,55 Дж/г, 97,99 Дж/г для ацетона и 58,99 Дж/г для метана. Обратите внимание, что вода имеет относительно высокую теплоту плавления по сравнению с другими. Следующее уравнение можно использовать для расчета тепловой энергии, связанной с процессом плавления.
(В этом контексте плавление – это другое слово для плавления.) Единицы для ΔH fus различаются, но обычно они описываются в Дж / г. Как и удельные теплоемкости, теплоты плавления варьируются от одного вещества к другому. Например, для воды она составляет 333,55 Дж/г, 97,99 Дж/г для ацетона и 58,99 Дж/г для метана. Обратите внимание, что вода имеет относительно высокую теплоту плавления по сравнению с другими. Следующее уравнение можно использовать для расчета тепловой энергии, связанной с процессом плавления. )
) Например, теплота конденсации воды составляет -2257 Дж/г.
Например, теплота конденсации воды составляет -2257 Дж/г. Температура является мерой средней внутренней кинетической энергии вещества, поэтому, если кинетическая энергия не увеличивается, то не увеличивается и температура. Расчеты, относящиеся к процессу плавления, можно выполнить с помощью следующего уравнения.
Температура является мерой средней внутренней кинетической энергии вещества, поэтому, если кинетическая энергия не увеличивается, то не увеличивается и температура. Расчеты, относящиеся к процессу плавления, можно выполнить с помощью следующего уравнения. Расчеты, относящиеся к процессу парообразования, можно выполнить с помощью следующего уравнения.
Расчеты, относящиеся к процессу парообразования, можно выполнить с помощью следующего уравнения. Учащийся знает, что изменения происходят в физической системе, и применяет законы сохранения энергии и импульса. Ожидается, что студент:
Учащийся знает, что изменения происходят в физической системе, и применяет законы сохранения энергии и импульса. Ожидается, что студент: Следовательно, он поглощает больше энергии из смеси мороженого.
Следовательно, он поглощает больше энергии из смеси мороженого.