Буферная емкость Lavoro 500 ГВС
Бак теплоаккумулятор (буферная емкость) Lavoro c ГВС предназначен для использования в системах отопления с возможностью получения ГВС. Емкость накапливает и сохраняет избытки тепловой энергии от различных источников тепла, т.е. если Вам необходима совместная работа нескольких источников тепла, например, Вы хотите объединить работу твердотопливного котла и электрического котла, или газового котла и дровяного котла, или теплового насоса и твердотопливного котла и электрического котла, и так далее.
Хорошо сочетает следующие источники тепла
- Твердотопливный котел
- Котел на биомассе
- Пеллетный котел
- Камин с водяной рубашкой
- Тепловой насос
- Газовый котел
- Электрический котел
Теплообменник контура ГВС выполнен из высококачественной нержавеющей стали марок AISI304 и AISI 316 L. С такой системой вы не будете думать о замене магниевых анодов каждые 0,5- 1 год.
С такой системой вы не будете думать о замене магниевых анодов каждые 0,5- 1 год.
Теплоаккумулятор Lavoro изготовлен из углеродистой стали толщиной 2-5 мм. Изоляция бака выполнена по технологии NOFIRE из полиэфирного материала толщиной 70 мм, поддающегося 100% вторичной переработке (экологически безопасный материал), материал обладает высоким коэффициентом сопротивления теплопередачи, а так же высоким классом огнестойкости класса B-s2d0 в соответствии с Европейскими требованиями EN 13501.
Теплоаккумуляторы рассчитаны на рабочую температуру с использованием воды и водно-гликолевых, а также спиртовых растворов от +2 до +95 градусов по Цельсию.
Внешняя сторона бака окрашена термостойкой краской способной выдерживать динамические изменения температуры.
Нижняя опора бака выполнена по принципу кольцевой опоры, позволяющей равномерно распределять вес бака на поверхность пола и обеспечить устойчивость.
Все баки оснащены подводящими и отводящими штуцерами, выполненными из бесшовной толстостенной трубы.
Опционально доступно
- Бак может быть изолирован эластичным пенополиуретаном толщиной 70 мм, а с наружной стороны защищен матерчатой изоляцией.
- Внутренняя поверхность бака может быть покрыта цинковым
составом, для возможности хранения в баке горячей
технической воды.
Технические характеристики
| Объем | 500 л |
| Высота | 1570 мм |
| Диаметр | 780 мм |
| Максимальная температура в баке | 95 С |
| Рабочее давление бака | 3 бар |
| Испытательное давление бака | 9 бар |
| Максимальное давление теплообменника | 6 бар |
| Рабочее давление теплообменника | 6 бар |
| Внутренний диаметр трубы теплообменника | 27 мм |
| Максимальная температура теплообменника | 110 С |
| Площадь теплообменника | 2,7 м2 |
| Рекомендуемая мощность котла | 44 кВт |
Производительность теплообменника при темп. бака 65 С (65/10/45) бака 65 С (65/10/45) | 1350 л/ч |
| Масса | 115 кг |
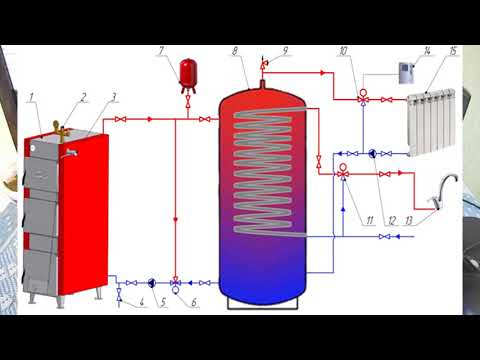
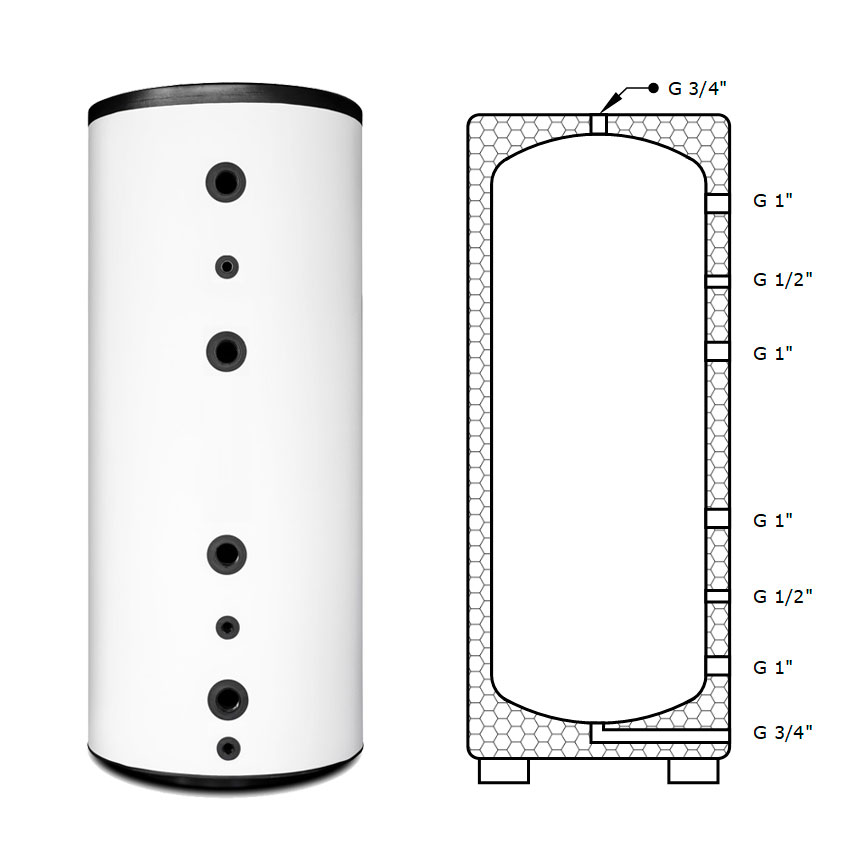
Буферная емкость S-TANK AT 1200
Буферная емкость S-Tank AT 1200 для котла системы отопления.
Буферный теплоаккумулятор Белорусского производства S-Tank AT 1200, представляет собой емкость без теплообменника объемом 1200 литров.
Поверх буферного бака надета теплоизоляция толщиной 70мм. Теплоизоляция закрыта кожухом из пластика на алюминиевой защелке. Теплоизоляционный кожух может быть легко демонтирован, и также установлен обратно на теплоаккумулятор для удобства монтажа и транспортировки.
Данный объем, как правило, подходит для котлов мощностью около 40 кВт. Следовательно, для достаточно небольших помещений. Более подходящим теплогенератором для такого объема теплоносителя будет являться твердотопливный котел малой мощности.
Теплоаккумулятор 1200 литров
Теплоаккумулятор S-Tank AT 1200 имеет восемь отверстий для подключения и отдачи котловой воды, диаметром 1 ½» с внутренней резьбой, расположенных под углом 90 градусов на различной высоте буферного накопителя. Это делает его очень удобным для подключения разных контуров отопления или подготовки ГВС. Также такое расположение патрубков позволяет установить накопительный теплоаккумулятор в угол помещения / котельной.
Это делает его очень удобным для подключения разных контуров отопления или подготовки ГВС. Также такое расположение патрубков позволяет установить накопительный теплоаккумулятор в угол помещения / котельной.
Еще на буферной емкости расположено 4 отверстия диаметром 1/2» для монтажа термоманометров или каких-то других терморегулирующих датчиков.
Рабочее давление буферной емкости 3 атм. Такого давления вполне достаточно для нормальной работы аккумулятора тепла в системе отопления.
Белорусское производственное предприятие S-TANK гарантирует соответствие емкостей модельного ряда АТ требованиям безопасности, при условии соблюдения правил монтажа, эксплуатации и транспортировки.
Гарантийный срок составляет 5 лет со дня продажи.
174.00 кг
Размеры (Д x Ш x В):
1,070.00 x 1,070.00 x 2,010.00 мм
Серия теплоаккумулятора:
AT
org/PropertyValue”>Котел , кВт:
40
Без теплообменника
Давление, max , Атм:
6
Диаметр без теплоизоляциии , мм:
940
Производство:
Белоруссия
Гарантия , мес:
60
Объем, л:
1200
7.
 2: Практические аспекты буферов
2: Практические аспекты буферов- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 164772
Развитие навыков
- Понимание факторов, влияющих на диапазон и емкость буфера
- Рассчитать количества кислоты и основания, необходимые для приготовления буфера с заданным рН
Буферы характеризуются диапазоном рН, в котором они могут поддерживать более или менее постоянное значение рН, и их буферной емкостью, т. е. количеством сильной кислоты или основания, которое может быть абсорбировано до того, как рН значительно изменится. Хотя полезный диапазон pH буфера сильно зависит от химических свойств слабой кислоты и слабого основания, используемых для приготовления буфера (т.
Буферная емкость
Буферные растворы не обладают неограниченной емкостью для поддержания относительно постоянного уровня pH (Рисунок \(\PageIndex{1}\)). Если мы добавим в буфер такое количество основания, что слабая кислота будет исчерпана, буферное действие по отношению к основанию будет невозможно. С другой стороны, если мы добавим избыток кислоты, слабое основание будет исчерпано, и буферное действие по отношению к любой дополнительной кислоте будет невозможно. На самом деле нам даже не нужно исчерпать всю кислоту или основание в буфере, чтобы переполнить его; его буферное действие будет быстро уменьшаться по мере того, как данный компонент приближается к истощению.
Рисунок \(\PageIndex{1}\): Цвет индикатора (метиловый оранжевый) показывает, что небольшое количество кислоты, добавленное к буферному раствору с pH 8 (стакан слева), мало влияет на буферную систему (средний стакан).
Буферная емкость — это количество кислоты или основания, которое можно добавить к заданному объему буферного раствора до того, как рН значительно изменится, обычно на одну единицу. Буферная емкость зависит от количества слабой кислоты и сопряженного с ней основания, находящихся в буферной смеси.
Чем более концентрирован буферный раствор, тем больше его буферная емкость.
Как показано на рисунке \(\PageIndex{2}\), при добавлении \(NaOH\) к растворам, содержащим разные концентрации буфера уксусной кислоты/ацетата натрия, наблюдаемое изменение рН буфера обратно пропорционально пропорциональна концентрации буфера. Если буферная емкость в 10 раз больше, то буферный раствор может поглотить в 10 раз больше сильной кислоты или основания, прежде чем претерпит значительное изменение рН.
Рисунок \(\PageIndex{2}\): Влияние концентрации буфера на емкость буфера Буфер поддерживает относительно постоянное значение pH при добавлении в раствор кислоты или основания. Добавление даже крошечных объемов 0,10 М \(NaOH\) к 100,0 мл дистиллированной воды приводит к очень большому изменению рН. По мере увеличения концентрации смеси буфера ацетата натрия/уксусной кислоты в соотношении 50:50 в растворе с 0,010 М до 1,00 М изменение рН, вызываемое добавлением того же объема раствора \(NaOH\), неуклонно уменьшается. . При концентрации буфера не менее 0,500 М добавление даже 25 мл раствора \(NaOH\) приводит лишь к относительно небольшому изменению рН.
Добавление даже крошечных объемов 0,10 М \(NaOH\) к 100,0 мл дистиллированной воды приводит к очень большому изменению рН. По мере увеличения концентрации смеси буфера ацетата натрия/уксусной кислоты в соотношении 50:50 в растворе с 0,010 М до 1,00 М изменение рН, вызываемое добавлением того же объема раствора \(NaOH\), неуклонно уменьшается. . При концентрации буфера не менее 0,500 М добавление даже 25 мл раствора \(NaOH\) приводит лишь к относительно небольшому изменению рН.
Диапазон буфера
Диапазон буфера — это диапазон значений pH, при котором буфер наиболее эффективен (т. е. имеет наибольшую буферную емкость для своей концентрации). Хорошая буферная смесь должна иметь примерно равные концентрации обоих компонентов. Как правило, буферный раствор теряет свою полезность, когда один компонент буферной пары составляет менее 10% от другого. На рисунке \(\PageIndex{3}\) показан буфер уксусной кислоты и ацетат-иона при добавлении основания. Начальное значение pH равно 4,74 (pK_a\ уксусной кислоты). Изменение на 1 единицу pH происходит, когда концентрация уксусной кислоты снижается до 11% от концентрации ионов ацетата. После этой точки рН начинает меняться быстрее при добавлении основания, поскольку буфер переполняется.
Изменение на 1 единицу pH происходит, когда концентрация уксусной кислоты снижается до 11% от концентрации ионов ацетата. После этой точки рН начинает меняться быстрее при добавлении основания, поскольку буфер переполняется.
Рисунок \(\PageIndex{3}\): График, иллюстрирующий буферное действие, показывает изменение рН по мере добавления увеличивающегося количества 0,10 М раствора NaOH к 100 мл буферного раствора, в котором изначально [CH 3 CO 2 H] = 0,10 М и \(\ce{[Ch4CO2- ]}=0,10\:M\)
Наиболее эффективные буферы содержат равные концентрации кислоты и сопряженного с ней основания.
Буфер, который содержит примерно равные количества слабой кислоты и сопряженного с ней основания в растворе, одинаково эффективен для нейтрализации добавленного основания или добавленной кислоты. Это показано на рисунке \(\PageIndex{4}\) для буфера уксусная кислота/ацетат натрия. Добавление данного количества сильной кислоты смещает систему по горизонтальной оси влево, а добавление такого же количества сильного основания смещает систему на такое же расстояние вправо. -\) к \(CH_3CO_2H\) с 1:1 снижает буферную емкость раствора.
-\) к \(CH_3CO_2H\) с 1:1 снижает буферную емкость раствора.
Напомним, что в соответствии с соотношением Хендерсона-Хассельбаха pH = \(pK_a\), когда буфер содержит равные концентрации конъюгированной кислоты и основания. Таким образом, эффективный диапазон буфера составляет примерно \(pK_a\) плюс или минус одна единица pH. Это соответствует концентрации двух компонентов десять к одному в любом случае, как показано выше.
Диапазон буфера приблизительно равен \(pH = pK_a \pm 1\)
Подготовка буферов
Во многих случаях химикам приходится готовить буферные растворы для поддержания желаемого уровня pH.
- Выберите подходящую буферную систему. Поскольку буферная емкость самая высокая при pH = \(pK_a\), идеальный буфер будет иметь \(pK_a\), близкий к желаемому pH. В общем, слабые кислоты и их соли лучше подходят в качестве буферов при рН менее 7; слабые основания и их соли лучше подходят в качестве буферов при рН выше 7.
- Используйте общую концентрацию буфера и желаемый рН для расчета количеств кислоты и основания, необходимых для создания буфера. Уравнение Хендерсона-Хассельбаха можно использовать для определения необходимого соотношения [основания]/[кислоты].
- Смешайте компоненты.

- Отрегулируйте pH по желанию. На практике экспериментальная ошибка и другие факторы часто приводят к тому, что буферы не совсем соответствуют расчетному pH, поэтому химик может добавить небольшое количество сильной кислоты или сильного основания для точной настройки pH, контролируя раствор с помощью pH-метра.
Пример \(\PageIndex{1}\) иллюстрирует метод расчета количества реагентов, необходимых для создания буфера с заданным значением pH.
Пример \(\PageIndex{1}\)
\(pK_a\) муравьиной кислоты составляет 3,75. Сколько граммов муравьиной кислоты (\(HCO_2H\)) и формиата натрия (\(HCO_2Na\)) необходимо смешать, чтобы приготовить 100,0 мл буфера с общей концентрацией 0,100 М и рН 3,90?
Дано : \(pK_a\) муравьиной кислоты, объем буфера, общая концентрация буфера, желаемый pH
Запрашиваемый : граммы \(HCO_2H\) и \(HCO_2Na\)
Стратегия 1 : Используйте приближение Хендерсона-Хассельбаха, чтобы определить необходимое соотношение [основание]/[кислота], затем используйте общую концентрацию и объем для расчета количества молей каждого необходимого компонента, конвертируйте моли в граммы
Решение:
Согласно приближению Хендерсона-Хассельбальха, 9{0,15} = 1,16\]
Это соотношение означает, что буфер должен содержать в 1,16 раза больше молей \(HCO_2Na\), чем \(HCO_2H\), чтобы получить pH 3,90. Это имеет смысл, потому что желаемый pH выше, чем \(pK_a\), поэтому необходимо больше сопряженного основания, чем кислоты.
Это имеет смысл, потому что желаемый pH выше, чем \(pK_a\), поэтому необходимо больше сопряженного основания, чем кислоты.
Мы знаем, что нам нужно создать 100,0 мл буфера с общей концентрацией 0,100 М:
\(\mathrm{100,0 мл×\dfrac{1 л}{1000 мл}×\dfrac{0,100 моль}{1 L}= 0,0100\:моль}\)
Таким образом, нам нужно всего 0,0100 моль обоих компонентов буфера. Мы можем составить следующие два уравнения:
\(\mathrm{моль(HCO_2Na) + моль(HCO_2H) = 0,0100\:моль}\)
\(\mathrm{моль(HCO_2Na)/моль(HCO_2H) = 1,16}\) или \(\mathrm {моль(HCO_2Na) = 1,16×моль(HCO_2H)}\)
С двумя уравнениями и двумя неизвестными подставляем одно выражение в другое, чтобы найти оба компонента:
\(\mathrm{1,16×моль(HCO_2H) + моль(HCO_2H) = 2,16×моль(HCO_2H) = 0,0100\:моль}\)
\(\mathrm{моль(HCO_2H) = 0,00463\:моль\:HCO_2H}\)
\(\mathrm{моль (HCO_2Na) = 1,16×0,00463\:моль = 0,00537\:моль\:HCO_2Na}\)
Наконец, вычисляем граммы, используя молярную массу каждого компонента: \:г\:HCO_2H}\)
\(\mathrm{0,00537\:моль\:HCO_2Na×\dfrac{68,01\:г}{1\:моль\:HCO_2Na}=0,365\:г\:HCO_2Na} \)
Упражнение \(\PageIndex{1}\)
Биохимику требуется 250 мл 0,15 М ацетатно-уксусного буфера с рН 5,00.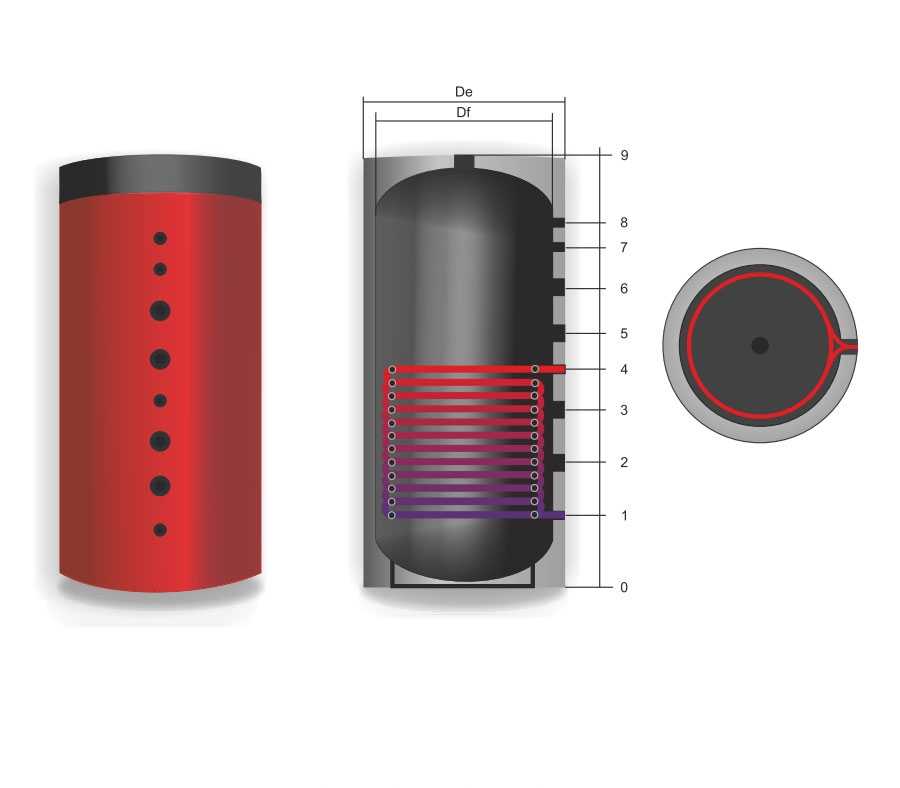 Сколько граммов \(CH_3CO_2H\) и \(CH_3CO_2Na\) она должна добавить, чтобы создать буферную смесь (\(pK_a\) уксусной кислоты 4,74)?
Сколько граммов \(CH_3CO_2H\) и \(CH_3CO_2Na\) она должна добавить, чтобы создать буферную смесь (\(pK_a\) уксусной кислоты 4,74)?
- Ответить
0,98 г \(CH_3CO_2H\) и 1,74 г \(CH_3CO_2Na\)
Резюме
Буферы характеризуются диапазоном pH и буферной емкостью. Полезный диапазон pH буфера зависит от химических свойств сопряженной пары слабых кислот и оснований, используемой для приготовления буфера, и обычно равен \(pK_a \pm 1\). Буферная емкость зависит от концентрации частиц в растворе; чем более концентрирована буферная смесь, тем выше буферная емкость. Буфер имеет наибольшую емкость при равных концентрациях слабой кислоты и сопряженного основания, когда \(pH = pK_a\).
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Лицензия
- CC BY-NC-SA
- Показать страницу TOC
- нет на странице
- Теги
- буфер
- емкость буфера
- приближение Хендерсона-Хассельбаха
- источник-хим-25184
- зрительский ион
Емкость буфера — PubMed
Обзор
. 2018;54:11-18.
2018;54:11-18.
дои: 10.1159/000489513. Epub 2018 21 августа.
Эрхардт Прокш
- PMID: 30130768
- DOI: 10.1159/000489513
Обзор
Эрхардт Прокш. Курр Пробл Дерматол. 2018.
. 2018;54:11-18.
дои: 10.1159/000489513. Epub 2018 21 августа.
Автор
Эрхардт Прокш
- PMID: 30130768
- DOI:
10.
 1159/000489513
1159/000489513
Абстрактный
Каждая биологическая система имеет широко неизвестную буферную систему для поддержания кислотно-щелочного баланса на определенном уровне pH. Наша жизнь зависит от функционирования буферных систем. Буферная система представляет собой раствор, устойчивый к изменению pH при добавлении кислот или оснований. Кожа обладает достаточно высокой буферной емкостью, которая определяется количеством ионов Н+ или ОН-, которое необходимо до тех пор, пока значение рН раствора не изменится на единицу. Буферы содержат слабую или среднесильную кислоту (основание) и соответствующую соль. Буферы, которые показывают pKa в диапазоне pH поверхности рогового слоя, наиболее важны для кожи. Буферная емкость снижена как у детской, так и у возрастной кожи. Внешние факторы, вода и моющие средства могут снизить локальную буферную емкость из-за вымывания буферных химических веществ, что приводит к повышению рН и раздражающему контактному дерматиту. Воспалительные заболевания, включая атопический дерматит, псориаз и вульгарные угри, которые показывают повышенный рН, вероятно, также должны иметь сниженную буферную способность. Для лечения кожных заболеваний и стареющей кожи следует предпочтительно использовать эмоленты с pH, немного более кислым, чем средний нормальный pH, и с соответствующей буферной емкостью.
Воспалительные заболевания, включая атопический дерматит, псориаз и вульгарные угри, которые показывают повышенный рН, вероятно, также должны иметь сниженную буферную способность. Для лечения кожных заболеваний и стареющей кожи следует предпочтительно использовать эмоленты с pH, немного более кислым, чем средний нормальный pH, и с соответствующей буферной емкостью.
© 2018 S. Karger AG, Базель.
Похожие статьи
Кислотная мантия: миф или неотъемлемая часть здоровья кожи?
Сурбер С., Гумберт П., Абельс С., Майбах Х. Сурбер С и др. Курр Пробл Дерматол. 2018;54:1-10. дои: 10.1159/000489512. Epub 2018 20 августа. Курр Пробл Дерматол. 2018. PMID: 30125885 Рассмотрение.
Измерение буферной способности кожи человека: модель in vitro.

Чжай Х., Чан Х.П., Фарахманд С., Майбах Х.И. Чжай Х и др. Технология восстановления кожи. 2009 ноябрь; 15 (4): 470-5. doi: 10.1111/j.1600-0846.2009.00392.x. Технология восстановления кожи. 2009. PMID: 19832960
Рубцовые буферы: временное влияние на буферную способность и рН рубцовой жидкости у коров, получавших рацион с высоким содержанием концентратов.
Ле Руйе П., Такер В.Б. Ле Руйе П. и др. Дж. Молочная наука. 1992 г., апрель 75(4):1069-77. doi: 10.3168/jds.S0022-0302(92)77851-5. Дж. Молочная наука. 1992. PMID: 1315810
рН и микробные инфекции.
Риппке Ф., Берардеска Э., Вебер ТМ. Риппке Ф. и др. Курр Пробл Дерматол. 2018;54:87-94. дои: 10.1159/000489522. Epub 2018 21 августа.
 Курр Пробл Дерматол. 2018.
PMID: 30130777
Рассмотрение.
Курр Пробл Дерматол. 2018.
PMID: 30130777
Рассмотрение.Буферная способность слоев кожи человека: in vitro.
Чжэн Ю., Сотоодян Б., Лай В., Майбах Х.И. Чжэн И и др. Технология восстановления кожи. 2012 Февраль; 18 (1): 114-9. doi: 10.1111/j.1600-0846.2011.00543.x. Epub 2011 3 мая. Технология восстановления кожи. 2012. PMID: 21535188
Посмотреть все похожие статьи
Цитируется
Модель многофазной многоуровневой механистической кожной абсорбции (MPML MechDermA) для прогнозирования местного и системного воздействия лекарственных препаратов, наносимых на кожу.
Патель Н., Кларк Дж. Ф., Салем Ф., Абдулла Т., Мартинс Ф., Арора С., Цакалозу Э., Ходжкинсон А.



 1159/000489513
1159/000489513
 Курр Пробл Дерматол. 2018.
PMID: 30130777
Рассмотрение.
Курр Пробл Дерматол. 2018.
PMID: 30130777
Рассмотрение.